Le ribosome, véritable usine moléculaire de la cellule, est responsable de la traduction du code génétique en protéines, un processus fondamental pour la vie. La formation de cet organite essentiel, appelée biogenèse ribosomique, est un processus d'une complexité remarquable, nécessitant une coordination précise pour produire rapidement des sous-unités ribosomiques matures et fonctionnelles. Toute défaillance dans ce processus, qu'il s'agisse de mutations dans ses composants ou de dysfonctionnements lors de son assemblage, peut avoir des conséquences désastreuses, conduisant à diverses pathologies telles que des anémies, des retards de croissance, voire certains types de cancers. Par conséquent, une compréhension approfondie des mécanismes d'assemblage et de fonctionnement des ribosomes, tant dans les conditions physiologiques que pathologiques, revêt une importance primordiale.
La Structure et la Composition du Ribosome
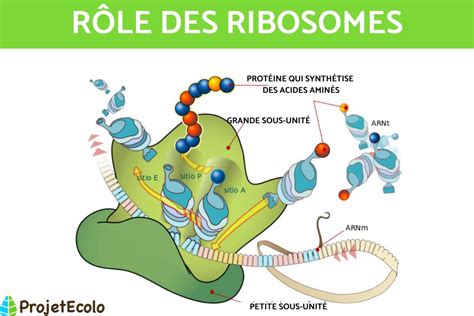
Le ribosome est un complexe ribonucléoprotéique (RNP) de très grande taille, dont la structure est remarquablement conservée à travers le règne vivant. Il est composé de quatre ARN ribosomiques (ARNr) et d'environ 80 protéines ribosomiques, organisés en deux sous-unités distinctes : la petite sous-unité (40S chez les eucaryotes) et la grande sous-unité (60S chez les eucaryotes).
La petite sous-unité, constituée de l'ARNr 18S et de 33 protéines ribosomiques, joue un rôle central dans l'activité de décodage de l'ARN messager (ARNm). Elle est essentielle pour la reconnaissance précise du codon sur l'ARNm et de l'anticodon sur l'ARN de transfert (ARNt), garantissant ainsi la fidélité de la traduction de l'information génétique.
La grande sous-unité, quant à elle, est responsable de la formation de la liaison peptidique. Elle comprend trois ARNr (5S, 5.8S et 28S chez les eucaryotes) et 47 protéines ribosomiques. C'est au sein de son centre peptidyl-transférase que la chaîne d'acides aminés est synthétisée, formant ainsi la protéine naissante. Le peptide en cours de formation quitte ensuite le ribosome par un tunnel de sortie, où il est pris en charge par des chaperons protéiques qui facilitent son repliement correct.
La Biogenèse Ribosomique : Un Processus Hiérarchisé et Régulé
La biogenèse des ribosomes est un processus dynamique et hautement coordonné, qui débute dans le nucléole, une structure spécialisée du noyau cellulaire. Chez les eucaryotes, ce processus est particulièrement complexe et a fait l'objet d'études approfondies, notamment chez la levure Saccharomyces cerevisiae, un organisme modèle particulièrement adapté pour les recherches génétiques et biochimiques. Bien que le modèle de biogenèse de la levure soit largement conservé chez les eucaryotes supérieurs, des différences notables existent, tant au niveau structurel qu'en ce qui concerne les acteurs protéiques impliqués.
La synthèse de trois des quatre ARNr (18S, 5.8S et 28S) se fait dans le nucléole sous la forme d'un long ARN précurseur, le pré-ARNr 47S, transcrit par l'ARN polymérase I. L'ARNr 5S, quant à lui, est transcrit indépendamment par l'ARN polymérase III. Simultanément, les protéines ribosomiques sont traduites dans le cytoplasme et importées dans le nucléole pour s'assembler avec les ARNr naissants.
Ce processus d'assemblage implique une série complexe de clivages, de modifications chimiques des ARNr et de modifications post-traductionnelles des protéines ribosomiques. De nombreux facteurs d'assemblage, ainsi que des ARN hélicases, des ATPases et des GTPases, jouent un rôle crucial dans la remodélisation des précurseurs de sous-unités ribosomiques, fournissant l'énergie nécessaire à ces transformations moléculaires.
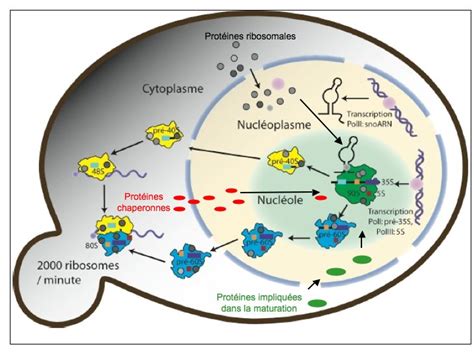
Au cours de leur maturation, les précurseurs des sous-unités ribosomiques (pré-40S et pré-60S) transitent du nucléole vers le cytoplasme, passant par le nucléoplasme et subissant des étapes finales de maturation avant de devenir pleinement fonctionnels. Ce voyage est étroitement régulé, avec un système de contrôle qualité qui assure que seules les particules suffisamment matures sont exportées.
Les Voies de Maturation des ARNr : Complexité et Alternatives
La maturation des ARNr, particulièrement celle des précurseurs de la petite sous-unité (pré-ARNr 18S), est un processus complexe impliquant de multiples étapes de clivage endonucléolytique et d'exonucléolytique. Le pré-ARNr 47S subit une série de clivages pour générer les ARNr matures 18S, 5.8S et 28S. Chez l'homme, deux voies principales de clivage coexistent.
Dans la voie majoritaire (environ 70% chez les cellules HeLa), le pré-ARNr 45S est d'abord clivé au site 2, séparant les précurseurs destinés à la petite et à la grande sous-unité (pré-ARNr 30S et 32S). Le pré-ARNr 30S est ensuite clivé pour former le pré-ARNr 21S, qui subit une maturation séquentielle médiée par l'exosome, conduisant finalement à l'ARNr 18S mature après un clivage final dans le cytoplasme.
La voie minoritaire (environ 30% chez les cellules HeLa) implique des clivages initiaux dans le 5'-ETS, générant le pré-ARNr 41S, qui est ensuite clivé au site 2 pour produire les pré-ARNr 21S et 32S, suivant ensuite les étapes décrites précédemment.
Il existe également des voies de clivage alternatives, notamment au niveau de l'ITS1, qui peuvent produire des intermédiaires comme le pré-ARNr 18S-E, précurseur direct de l'ARNr de la petite sous-unité. Ces variations soulignent la flexibilité et la complexité des mécanismes de maturation des ARNr.
Modifications des ARNr : Affinement Fonctionnel
Au-delà des clivages, les ARNr subissent de nombreuses modifications chimiques qui sont cruciales pour leur structure, leur stabilité et leur fonction au sein du ribosome. Ces modifications incluent des isomérisations d'uridine (pseudo-uridylation) et des méthylations de riboses et de bases nucléotidiques. La majorité de ces modifications se situent à proximité des sites fonctionnels du ribosome.
Les pseudo-uridylations et les méthylations des riboses sont guidées par des petits ARN nucléolaires (snoARN) qui interagissent avec des enzymes spécifiques, la fibrillarine et la dyskérine. Les snoARN, grâce à des séquences complémentaires, dirigent ces enzymes vers les positions précises à modifier sur l'ARNr cible. Les méthylations des bases nucléotidiques, quant à elles, sont réalisées par d'autres enzymes, dont certaines sont encore en cours d'identification. Ces modifications fines sont essentielles pour le bon fonctionnement du ribosome.
L'Export des Pré-ribosomes : Un Passage Contrôlé
L'export des précurseurs de sous-unités ribosomiques du noyau vers le cytoplasme est une étape cruciale et strictement régulée de la biogenèse ribosomique. Seules les particules ayant atteint un stade de maturation suffisant peuvent être transportées à travers les pores nucléaires. Ce contrôle est assuré en partie par l'assemblage de protéines ribosomiques spécifiques. Par exemple, la petite sous-unité n'est exportée que lorsque certaines protéines, telles que RPS15 et RPS5 (selon la nomenclature), sont correctement assemblées.
Certains facteurs d'assemblage agissent comme des adaptateurs, interagissant avec les exportines, des protéines chargées du transport nucléocytoplasmique. La protéine NMD3 est impliquée dans l'export des précurseurs de la grande sous-unité en recrutant l'exportine CRM1. Pour les précurseurs de la petite sous-unité, les facteurs d'assemblage RIOK2 et TSR1 seraient nécessaires pour interagir avec CRM1. L'interaction avec CRM1, facilitée par la protéine RAN-GTP, permet le passage des sous-unités à travers les pores nucléaires. D'autres karyophérines, comme le complexe TAP/p15, sont également impliquées dans ce transport.
Une fois dans le cytoplasme, les précurseurs de sous-unités ribosomiques font l'objet d'un dernier contrôle de qualité. Les facteurs d'assemblage des étapes finales inhibent les interactions non désirées entre les sous-unités elles-mêmes, ainsi qu'avec les ARNm et ARNt. Ce n'est qu'après avoir accompli leur rôle que ces facteurs sont libérés, permettant la formation du ribosome fonctionnel.
Le Rôle de YBEY dans la Biogenèse des Ribosomes
L'étude de la biogenèse ribosomique a révélé l'existence de facteurs protéiques essentiels, souvent hautement conservés. Parmi eux, la protéine YBEY, présente chez toutes les bactéries et chez certains eucaryotes possédant des organites d'origine bactérienne, joue un rôle critique. Dans tous les systèmes étudiés, YBEY est indispensable à la maturation des ARNr et à la biogenèse de la petite sous-unité ribosomique ; sa perte est généralement létale ou entraîne une débilité sévère.
Initialement, il a été proposé que YBEY agisse comme une endoribonucléase, clivant l'extrémité 3' de l'ARNr de la petite sous-unité. Cependant, cette hypothèse se heurte à plusieurs obstacles, notamment l'absence de spécificité de clivage observée pour YBEY et le manque de conservation phylogénétique des voies de processing des ARNr. De plus, chez certains organismes, l'absence de YBEY affecte les deux sous-unités ribosomiques, suggérant une activité qui n'est pas exclusivement limitée à la petite sous-unité. En résumé, bien que YBEY soit un facteur clé de la biogenèse ribosomique, son rôle exact reste sujet à débat.
Synthèse des protéines: Traduction
YBEY dans le Contexte Mitochondria
Des recherches sur l'orthologue humain de YBEY ont révélé sa localisation dans les mitochondries. Ce système génétique, hérité des bactéries, présente une particularité : les ARNr mitochondriaux sont séparés par des ARNt et ne nécessitent que les RNases P et Z pour leur traitement complet, rendant d'autres nucléases potentiellement superflues. Pourtant, l'invalidation (knockout) de YBEY dans les cellules humaines entraîne une déficience sévère de la traduction mitochondriale, compromettant la capacité de la cellule à respirer.
L'analyse des ARNr mitochondriaux a révélé une diminution significative de l'ARNr de la petite sous-unité, sans pour autant observer de défauts de processing. Des analyses par gradient de densité de saccharose à haute résolution ont mis en évidence des profils décalés des deux sous-unités mitochondriales, suggérant un manque de protéines et un arrêt à un stade intermédiaire d'assemblage. Ces observations indiquent que YBEY intervient dans la biogenèse des mitoribosomes non pas comme une nucléase, mais plutôt comme un facteur d'assemblage.
Interactions Moléculaires et Hypothèse sur le Rôle de YBEY
Les analyses d'interaction moléculaire ont établi que YBEY forme un complexe stable et stœchiométrique avec p32, une protéine de liaison à l'ARN mitochondriale. De plus, YBEY interagit avec un ensemble de protéines ribosomiques précoces de la grande sous-unité, une protéine spécifique de la petite sous-unité (uS11m), ainsi qu'avec ERAL1, un facteur critique de la biogenèse de la petite sous-unité.
Les mitoribosomes issus de cellules invalidées pour YBEY sont dépourvus d'uS11m et d'autres protéines des deux sous-unités, le manque d'uS11m étant particulièrement préjudiciable à l'initiation de la traduction. Sur la base de ces résultats, il est avancé l'hypothèse que YBEY agirait comme un facteur général de biogenèse des ribosomes. Il interviendrait à une étape précoce de l'assemblage de la grande sous-unité, puis déposerait la protéine ribosomique clé uS11m pour compléter l'assemblage de la petite sous-unité, assurant ainsi une stœchiométrie parfaite entre les deux sous-unités.
Perspectives de Recherche : Le Projet InsuRAF
Dans le cadre du projet InsuRAF, l'objectif est d'élucider les bases moléculaires de ce mécanisme unique par une approche intégrative combinant des méthodes phylogénétiques, génétiques, biochimiques, structurales et in situ. Il est attendu de pouvoir déterminer le mode, le contexte et la hiérarchie des interactions entre YBEY, p32, ERAL1, uS11m et d'autres composants ribosomiques, ainsi que de clarifier la mystérieuse activité enzymatique potentielle de YBEY.
Les données obtenues grâce au projet InsuRAF auront un impact significatif sur les domaines de la biologie des ribosomes, de la biologie de l'ARN mitochondrial et des disciplines associées, ouvrant de nouvelles perspectives pour la compréhension des processus cellulaires fondamentaux et de leurs implications dans la santé humaine. La caractérisation précise de ces mécanismes est essentielle, notamment compte tenu du rôle des ribosomes dans diverses maladies. Les avancées récentes en cryo-microscopie électronique (cryo-EM) ont considérablement amélioré notre capacité à résoudre les structures des ribosomes et de leurs précurseurs, permettant une description détaillée des mécanismes moléculaires impliqués dans leur biogenèse et leur fonctionnement.
Le Cas des Mutations Ribosomiques et des Maladies
Les mutations affectant les composants ribosomiques sont à l'origine de nombreuses pathologies humaines. Par exemple, des mutations ponctuelles dans le domaine C-terminal de la protéine ribosomique RPS15 ont été associées à divers types de leucémies et de tumeurs solides. Des études structurelles et fonctionnelles de ribosomes porteurs de telles mutations ont révélé une déstabilisation structurale de la protéine mutée, entraînant un ralentissement de l'étape d'élongation de la traduction. Ces découvertes soulignent le lien étroit entre l'intégrité structurale et fonctionnelle des ribosomes et la santé cellulaire, et renforcent l'importance de la recherche sur la biogenèse ribosomique.
L'étude des interactions entre l'ARN ribosomique et les protéines ribosomiques, par des techniques telles que les mesures de force par piège optique, permet de mieux comprendre les mécanismes d'assemblage. Ces expériences ont démontré que des protéines comme uL24 et uL4 peuvent stabiliser mécaniquement des fragments d'ARN 23S, mettant en lumière le rôle coopératif des protéines dans la structuration de l'ARN lors des premières étapes de l'assemblage de la grande sous-unité ribosomique. Ces observations, bien que réalisées sur des fragments d'ARN et dans des systèmes in vitro, apportent un éclairage précieux sur les principes fondamentaux de l'auto-assemblage des ribosomes.
tags: #assemblage #des #sous #unites #ribosomiques
