L'appareil de Golgi, également connu sous le nom de complexe de Golgi ou simplement Golgi, est un organite cellulaire vital présent dans toutes les cellules eucaryotes, qu'elles soient animales ou végétales. Sa structure complexe et sa localisation stratégique en font un acteur central dans le trafic vésiculaire, la modification et le tri des protéines et des lipides destinés à diverses destinations, qu'elles soient intracellulaires ou extracellulaires. L'histoire de sa découverte est jalonnée de controverses et d'avancées technologiques, reflétant la difficulté à appréhender cet organite dynamique.
Genèse d'une Découverte : Des Premières Observations à la Reconnaissance
L'histoire de l'appareil de Golgi commence en 1865 avec Adolph J.H.F. von La Valette-Saint George, un professeur d'anatomie de l'Université de Bonn. Dans ses travaux sur les cellules sexuelles de l'escargot, il décrit une structure qu'il nomme "Nebenkörper", dont l'évolution au cours de la mitose et sa reformation post-mitotique à partir d'une masse granulaire cytoplasmique sont observées. Bien qu'il soit possible que ce "Nebenkörper" corresponde à l'appareil de Golgi, cette identification n'a été faite que bien plus tard.
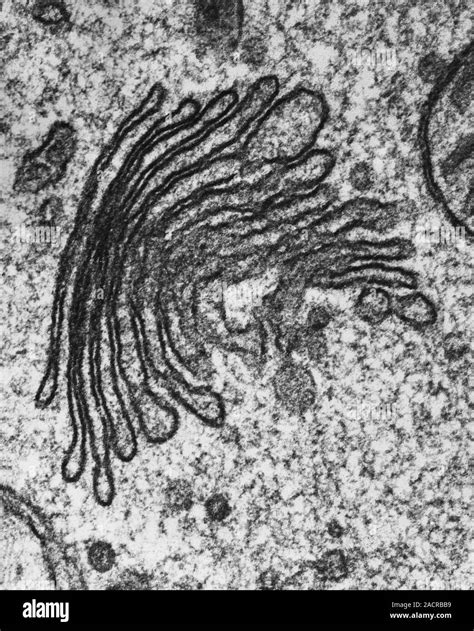
Le véritable tournant survient en 1896 lorsque Bartolomeo Camillo Emilio Golgi, de l'Université de Pavie, met au point une technique révolutionnaire de coloration des tissus nerveux. En expérimentant diverses méthodes d'imprégnation métallique, il découvre la "reazione nera", qui permet de visualiser les axones et les dendrites des cellules nerveuses en noir grâce au nitrate d'argent. C'est en utilisant cette technique, en 1898, sur des coupes de tissu nerveux de hibou et de chat, qu'il observe une structure intrigante à proximité du noyau et du centrosome : un "apparato reticolare interno".
L'anatomiste Friedrich Kopsch améliore la technique de coloration de Golgi en 1902, en y introduisant une imprégnation à l'acide osmique, créant ainsi une coloration mixte à l'osmium et au nitrate d'argent. En 1909, l'"apparato reticolare interno" est officiellement rebaptisé "appareil de Golgi", puis plus tard "complexe de Golgi".
Ironiquement, la découverte de ce nouvel organite passa relativement inaperçue, même lorsque Camillo Golgi et Santiago Ramon y Cajal partagèrent le prix Nobel de physiologie ou médecine en 1906 pour leurs travaux sur la structure du tissu nerveux. La reconnaissance de l'appareil de Golgi comme une entité cellulaire distincte fut un processus long et semé d'embûches.
Controverses et Avancées Technologiques : La Lutte pour la Reconnaissance
Peu d'organites ont fait l'objet d'autant de controverses que l'appareil de Golgi. Plusieurs raisons expliquent cette situation. Premièrement, la technique d'imprégnation par les sels métalliques, bien qu'innovante, donnait des résultats difficiles à reproduire, semant le doute quant à la nature réelle des structures observées. Deuxièmement, la structure même du Golgi est intrinsèquement complexe, associant des saccules, des vésicules et des tubules. Ses limites avec les organites voisins, notamment le réticulum endoplasmique, étaient difficiles à définir, alimentant les débats : où finissait le réticulum endoplasmique et où commençait le Golgi ?
Ces débats n'empêchèrent pas un réel engouement pour cet organite. Cependant, au milieu du XXe siècle, un demi-siècle après sa découverte, des microscopistes renommés comme George Palade et Albert Claude, du Rockefeller Institute for Medical Research, soutenaient encore que l'appareil réticulaire était un artefact de coloration, une simple formation myélinique. En 1954, Albert Claude mettait même en garde contre "some artefacts such as the Golgi apparatus" dans une communication à la Royal Society.
L'avènement du microscope électronique marqua la fin de ces controverses. L'examen de coupes ultra-fines de cellules d'épididyme de rat par Albert Dalton et Marie D. Felix, ainsi que celles de pancréas de souris par Fritiof S. Sjöstrand et V. Hanzon, révélèrent l'architecture caractéristique de l'appareil de Golgi : un empilement de sacs membranaires aplatis, appelés saccules, citernes ou lamelles, entourés de vésicules. En hommage au travail pionnier d'Albert Dalton, l'organite fut baptisé "The Dalton complex" en 1956.
Morphologie et Polarité : La Structure du Golgi
Le complexe de Golgi est un organite omniprésent dans les cellules eucaryotes. Sa morphologie, bien que globalement reconnue, présente une certaine variabilité selon le type cellulaire. Les premières observations ont permis d'établir plusieurs caractéristiques clés :
- Localisation : Le Golgi est généralement situé à proximité du noyau et du centrosome, se positionnant entre le réticulum endoplasmique et la membrane plasmique. Cette localisation est particulièrement marquée dans les cellules à forte activité sécrétoire, comme celles des glandes du tube digestif, où la sécrétion est concentrée à un pôle spécifique de la cellule.
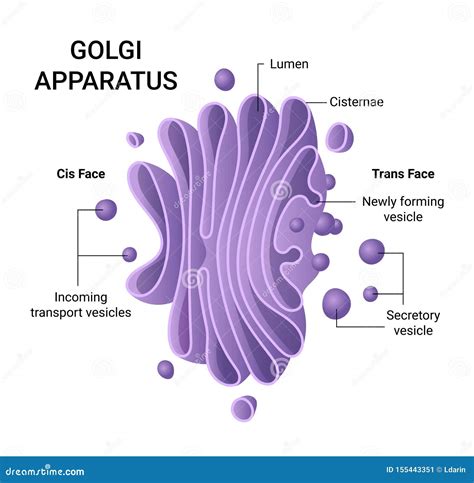
- Polarité cis-trans : Une caractéristique fondamentale du Golgi est sa polarité, décrite pour la première fois chez les flagellés par Pierre-Paul Grassé en 1957, puis chez les végétaux par Hilton H. Mollenhauer et Gordon Whaley en 1963. Cette polarité définit deux faces distinctes : la face cis (ou d'entrée), généralement tournée vers le réticulum endoplasmique, et la face trans (ou de sortie), orientée vers la membrane plasmique. Entre ces deux faces se trouvent les citernes médianes.
- Le Dictyosome : La structure golgienne la plus facilement reconnaissable est l'empilement de citernes, appelé "dictyosome". La forme de ces dictyosomes varie considérablement : des citernes ovales agencées en panier dans les cellules de l'épididyme, un réseau de rubans allongés dans les cellules des acini pancréatiques, ou encore une cage sphérique dans les cellules de l'hypophyse antérieure.
- Compartiments : Au sein du dictyosome, l'examen au microscope électronique et l'utilisation de réactifs cytochimiques ont permis de distinguer des saccules cis, médians et trans. La citerne cis est associée à une structure appelée réseau cis-golgien (CGN), formée par l'agrégation de vésicules provenant du réticulum endoplasmique. La citerne trans fait partie d'une structure complexe, le réseau trans-golgien (TGN).
Les premières tentatives de reconstruction tridimensionnelle du Golgi, entreprises par Albert Claude dans les années 1970, se heurtaient à des limitations technologiques. L'examen de coupes sériées au microscope électronique à transmission fournissait des données, mais l'absence de logiciels d'imagerie informatiques fiables empêchait une reconstitution précise.
Techniques d'Imagerie Avancées : La Révolution de la Microscopie
Les progrès significatifs dans les techniques de microscopie ont permis de lever le voile sur l'architecture délicate de l'appareil de Golgi. La microscopie électronique à balayage (MEB) a offert des images à haute résolution du Golgi à partir de coupes en série imprégnées à l'acide osmique.
Des avancées majeures dans la préservation de l'échantillon biologique ont également été réalisées. Les techniques de fixation actuelles bannissent l'utilisation de produits chimiques agressifs. L'échantillon est congelé dans l'azote liquide (-150°C) sous haute pression pour éviter la formation de cristaux aqueux. L'eau est ensuite remplacée par de la résine, infiltrée à basse température (-90°C), et après durcissement de la résine, les coupes sont préparées par cryo-ultra microtomie. Ces coupes peuvent ensuite être examinées par microscopie photonique à super-résolution, franchissant la limite de résolution des microscopes optiques conventionnels, ou par microscopie électronique à transmission.
L'obtention d'images tridimensionnelles à résolution nanométrique a été rendue possible par plusieurs approches :
- Techniques stéréoscopiques : L'examen de coupes ultra-fines (100 nanomètres) ou de coupes épaisses sous très hautes tensions (jusqu'à 3 000 000 de volts) par Alain Rambourg a permis d'obtenir des vues en trois dimensions.
- Tomographie électronique : Associée à la microscopie électronique, la tomographie électronique (dual-axis electron microscope tomography) offre également des reconstructions 3D précises.
Ces avancées ont permis de confirmer la présence de connexions tubulaires reliant les citernes au sein du dictyosome, une question qui a longtemps mobilisé l'attention des chercheurs. De telles connexions ont été décrites de manière convaincante dans diverses cellules, notamment les cellules ß de souris secrétant de l'insuline et les spermatides de rat.
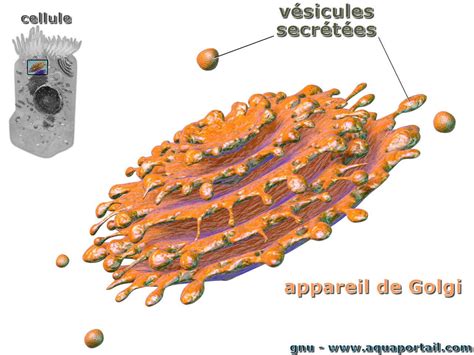
Fonctionnement et Flux Moléculaire : Le Golgi comme Centre de Tri
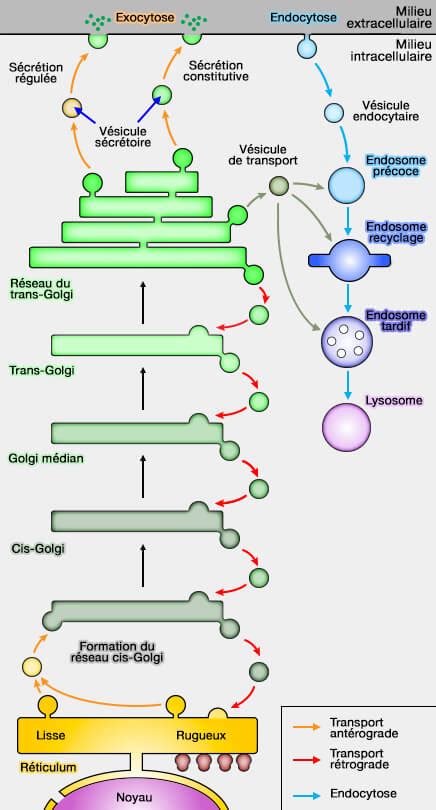
L'appareil de Golgi n'est pas une structure statique, mais un organite dynamique, constamment impliqué dans le trafic vésiculaire. Il représente un point de rencontre transitoire pour les lipides et protéines en route vers leurs destinations finales. Son existence est le résultat d'une production continue de vésicules de transport provenant du réticulum endoplasmique rugueux (RER), qui fusionnent pour former les citernes du côté cis-Golgi. Ce gain de membrane est compensé par une perte continue sous forme de vésicules de transport partant du côté trans.
Le RER et le Golgi sont interconnectés par un compartiment intermédiaire, l'ERGIC (Endoplasmic Reticulum-Golgi Intermediate Compartment), formé par la fusion de vésicules. Ce compartiment assure la liaison entre les deux organites.
Le fonctionnement du Golgi est caractérisé par un flux moléculaire constant :
- Compartiment intermédiaire (ERGIC) : Il se forme par agrégation de vésicules issues du RER, transportant des protéines et des lipides nouvellement synthétisés.
- Cis-Golgi Network (CGN) : Associé à la citerne cis, le CGN reçoit les vésicules du RER et initie le tri des molécules. Des enzymes comme la mannosidase-2 ou la galactosyltransférase, impliquées dans la glycosylation, y résident pendant environ 60 minutes.
- Citernes médianes : Le matériel progresse à travers les citernes médianes, où d'autres modifications biochimiques ont lieu.
- Trans-Golgi Network (TGN) : Situé à la sortie du Golgi, le TGN est une structure complexe où les molécules sont triées et empaquetées dans des vésicules destinées à des destinations spécifiques : sécrétion, lysosomes, ou retour vers le réticulum endoplasmique. Des protéines comme les SNAREs et de nombreux récepteurs n'y résident que pendant environ 10 minutes.
La plupart des protéines sécrétoires transitent dans les compartiments golgiens en environ 30 minutes, soulignant la rapidité et l'efficacité de ce processus.
LE SYSTEME ENDOMEMBRANAIRE : 🧫 Réticulum Endoplasmique, Appareil de Golgi, Lysosome, Endosome...
Fonctions Multiples : Au-delà du Simple Tri
Les fonctions de l'appareil de Golgi sont diverses et essentielles à la vie cellulaire :
- Maturation et Modification des Protéines et Lipides : Le Golgi est le site principal de modifications post-traductionnelles des protéines, telles que la glycosylation (ajout de chaînes de sucres) et la sulfatation. Il joue également un rôle crucial dans la synthèse et la modification des lipides, y compris la formation de sphingomyéline et de glycolipides. Le cis-Golgi fixe spécifiquement le marquage par l'osmium, comme l'ont démontré Daniel S. Friend et Michael J. Murray.
- Tri et Distribution : Le TGN agit comme un centre de tri sophistiqué, dirigeant les protéines et les lipides vers leurs destinations finales. Cela inclut leur inclusion dans des vésicules de sécrétion pour une libération à l'extérieur de la cellule (exocytose), leur livraison aux lysosomes, ou leur retour vers le réticulum endoplasmique.
- Synthèse de Macromolécules : Dans les cellules végétales, le Golgi est impliqué dans la synthèse de certains polysaccharides de la paroi cellulaire, tels que les pectines et les hémicelluloses.
- Formation des Lysosomes : Le Golgi est le lieu de biogenèse des lysosomes primaires, des vésicules contenant des enzymes hydrolytiques nécessaires à la dégradation des macromolécules et des organites endommagés.
- Renouvellement Membranaire : En participant à la voie sécrétoire et à l'endocytose, le Golgi contribue au renouvellement et à la régulation de la composition des membranes cellulaires.
- Rôle dans l'Exocytose : L'appareil de Golgi est un passage obligé et un régulateur du trafic vésiculaire qui aboutit à l'exocytose, le processus par lequel les cellules libèrent leur contenu à l'extérieur.
Le Pancréas : Un Modèle d'Activité Sécrétoire
Le pancréas, organe doté d'une activité sécrétoire élevée, offre un exemple classique de l'importance de l'appareil de Golgi. Le tissu exocrine du pancréas, constitué d'acini, synthétise et exporte une grande quantité d'enzymes digestives sous forme de précurseurs inactifs. Les cellules acineuses sont hautement polarisées : le noyau et le réticulum endoplasmique occupent la portion basale, tandis que le Golgi et les granules de sécrétion (grains de zymogènes) sont situés au pôle apical.
C'est dans les cellules des acini pancréatiques que George Palade, à la fin des années 1960, a brillamment mis en évidence l'existence de la voie sécrétoire, un processus fondamental impliquant le réticulum endoplasmique, le Golgi et les vésicules de sécrétion.
La Levure : Un Outil Génétique pour Décrypter la Voie Sécrétoire
Les travaux de Randy Schekman et de son étudiant Peter Novick sur les mutants des gènes SEC chez la levure Saccharomyces cerevisiae ont révolutionné notre compréhension de la voie sécrétoire. En utilisant ces mutants sensibles à la température, ils ont pu disséquer les étapes successives du transport vésiculaire. L'examen au microscope électronique de ces mutants a révélé l'accumulation de produits de sécrétion et de vésicules de sécrétion à différentes étapes du trafic, mettant en lumière le rôle crucial des gènes SEC dans la régulation de ce processus.
La technique des doubles mutants, inspirée par la notion de "létalité synthétique" de Theodosus Dobzhansky, a permis à Schekman et Novick de mettre en évidence les interactions entre les gènes impliqués dans des étapes similaires de la voie sécrétoire et de découvrir de nouvelles voies de signalisation. Par centrifugation en gradient de densité, ils ont pu séparer les cellules mutées et confirmer la séquence des étapes de la voie sécrétoire chez la levure, depuis la formation des vésicules à partir du réticulum endoplasmique jusqu'à leur fusion avec la membrane plasmique.
Purification et Caractérisation Biochimique : Les Défis de l'Analyse
La purification de l'appareil de Golgi pour en étudier la composition biochimique a longtemps représenté un défi majeur. Étant un composant relativement mineur de la cellule (environ 1% des protéines cellulaires dans les hépatocytes), son isolation par fractionnement subcellulaire (centrifugation différentielle et en gradient de densité) n'a pas été aisée.
Edward Kuff, Walter Schneider et Albert Dalton ont été parmi les premiers à utiliser ces techniques pour purifier l'appareil de Golgi d'épididyme de rat. Cependant, leurs analyses reposaient principalement sur des critères morphologiques, moins fiables en raison de la désagrégation de l'organite lors du broyage des tissus.
Ce n'est qu'en 1964 que Hilton H. Mollenhauer et James D. Morré ont résolu cette difficulté. En traitant les tissus à la glutaraldéhyde et en ajoutant un cation divalent (calcium) au milieu d'homogénéisation, ils ont réussi à conserver la morphologie et la polarité cis-trans du complexe. La même année, Sidney Goldfischer, E. Essner et Alex Novikoff ont mis au point un test histochimique révélant la présence de thiamine pyrophosphatase, une enzyme marqueur du Golgi.
Des études ultérieures, comme celle de Mary-Jane Spiro et Robert G. Spiro en 1968, ont permis d'isoler des enzymes spécifiques du Golgi, telles qu'une sialyltransférase catalysant le transfert d'acide sialique, contribuant ainsi à une meilleure compréhension de sa composition biochimique et de ses fonctions enzymatiques.
L'appareil de Golgi, loin d'être une simple structure statique, est un organite dynamique et essentiel à la vie cellulaire. Son histoire, marquée par des découvertes progressives et des controverses surmontées grâce aux avancées technologiques, témoigne de son importance capitale dans le fonctionnement des cellules eucaryotes. De la modification des protéines à la synthèse de macromolécules, en passant par le tri et le transport vésiculaire, le Golgi est un véritable carrefour moléculaire, orchestrant de nombreux processus vitaux.
tags: #cours #biologie #cellulaire #appareil #de #golgi
