Le développement d'un organisme multicellulaire est un processus d'une complexité fascinante, orchestré par une série de signaux et d'événements qui guident la formation des tissus, des organes et finalement d'un individu complet. Au cœur de cette orchestration se trouve la mise en place des axes de polarité du corps, des directions fondamentales qui définissent la structure tridimensionnelle de l'embryon. Chez les vertébrés, comme chez tous les bilatériens, trois axes principaux sont établis : l'axe antéro-postérieur (AP), l'axe dorso-ventral (DV) et l'axe droite-gauche. Ces axes ne sont pas de simples concepts anatomiques ; ils sont le résultat d'une cascade d'événements moléculaires et cellulaires qui débutent très tôt dans le développement, dès la formation de l'ovocyte et se poursuivent tout au long de l'embryogenèse.
L'Organisateur de Spemann : Un Centre Clé de la Morphogenèse
La coordination de la mise en place de ces axes chez les vertébrés repose sur une structure fondamentale connue sous le nom d'organisateur de Spemann. Cette région, identifiée pour la première fois par Hans Spemann et Hilde Mangold en 1924, joue un rôle crucial dans l'induction des structures embryonnaires dorsales et dans la définition de l'axe dorso-ventral, mais son influence s'étend également à la mise en place de l'axe antéro-postérieur et à l'établissement de l'asymétrie droite-gauche. Chez les amphibiens, l'organisateur de Spemann correspond à la lèvre dorsale du blastopore, tandis que chez les amniotes (comme les oiseaux et les mammifères), il est représenté par le nœud de Hensen.
L'expérience emblématique de Spemann et Mangold a démontré le pouvoir inducteur de la lèvre dorsale du blastopore. En greffant cette région d'une jeune gastrula d'amphibien sur la région ventrale d'un autre embryon, ils ont observé le développement d'un embryon secondaire, caractérisé par la présence de deux axes dorsaux, c'est-à-dire deux tubes neuraux, deux cordes dorsales et deux séries de somites. Cette expérience a révélé que la lèvre dorsale du blastopore, bien qu'elle se développe en corde dorsale, a la capacité d'induire les tissus environnants à former des structures nerveuses et des somites. Sans cette induction, les tissus ventraux auraient normalement donné naissance à de l'épiderme et à du mésoderme ventral, comme des cellules sanguines.

Des expériences ultérieures, comme celle de Gimlich et Gerhart, ont montré que les événements menant à la formation de l'organisateur de Spemann sont initiés très précocement dans l'embryon. La transplantation d'un macromère dorsal précoce (D1) vers la région ventrale d'un embryon de xénope à 32 cellules, tout en conservant le macromère dorsal d'origine (D1'), a également provoqué une duplication d'axe dorsal, soulignant l'importance de ces précurseurs dans la mise en place de l'organisateur.
L'Origine de la Polarité : La Rotation Corticale et la Voie Wnt
La genèse de la polarité embryonnaire remonte souvent à des événements qui se produisent avant même la segmentation de l'œuf. Chez les amphibiens, la fécondation déclenche une "rotation corticale" qui joue un rôle déterminant. Suite à la pénétration du spermatozoïde, le cortex de l'ovocyte, la couche cytoplasmique juste sous la membrane plasmique, se déplace d'environ 30 degrés dans la direction opposée au point d'entrée du spermatozoïde. Ce mouvement crée une zone dorsale distincte, souvent caractérisée par une apparence plus claire, connue sous le nom de croissant gris. La future région dorsale de l'embryon sera ainsi définie par cette rotation.
Cette rotation n'est pas qu'un simple déplacement de pigments. Elle implique le mouvement de molécules clés, telles que la protéine Dishevelled (Dsh), qui est transportée sur des microtubules. Dishevelled joue un rôle crucial dans la stabilisation de la β-caténine, une protéine essentielle à la signalisation Wnt, en la protégeant de la dégradation. La voie de signalisation Wnt, activée par des ligands comme Xwnt11, est ainsi favorisée du côté dorsal. L'accumulation de β-caténine dans le cytoplasme dorsal, puis son entrée dans le noyau à un stade précoce de la segmentation, est fondamentale pour l'établissement de la polarité dorsale. La β-caténine, en s'associant à des facteurs de transcription comme LEF/TCF, active l'expression de gènes essentiels au développement dorsal.
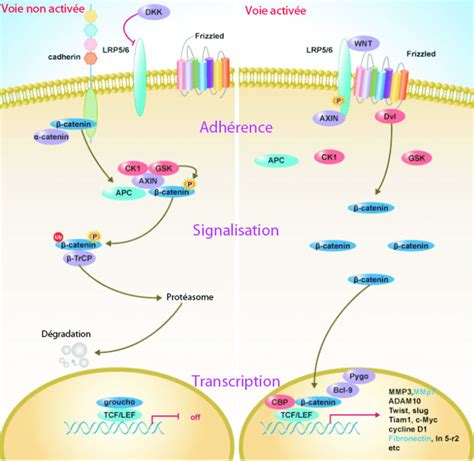
La mise en place de l'organisateur de Spemann résulte de la convergence de deux voies de signalisation complémentaires : la voie de la β-caténine, activée par la rotation corticale du côté dorsal, et la voie Nodal (ou Xnr chez le xénope). L'expression des ligands de Nodal, activée dans l'endoderme par le facteur de transcription VegT, est également cruciale. Une forte concentration de Xnr est nécessaire pour induire le mésoderme dorsal, qui forme l'organisateur. L'injection de β-caténine dans des cellules ventrales peut induire la formation d'un deuxième axe corporel, démontrant son rôle dans la dorsalisation. De même, l'incubation d'embryons dans une solution de chlorure de lithium (LiCl) a des effets dorsalisants et antériorisants.
L'expression différentielle des gènes Xnr, plus élevée du côté dorsal, crée un gradient de ce morphogène. La région marginale dorsale, recevant plus de Xnr, est induite en mésoderme dorsal, donnant naissance à l'organisateur de Spemann. C'est le centre de Nieuwkoop, situé dans l'endoderme dorsal, qui exprime le plus de Xnr et est capable d'induire un organisateur. Les blastomères végétatifs ventraux, sécrétant moins de Xnr, induisent du mésoderme ventral. L'activation de l'expression de Xnr5 et Xnr6 dans l'endoderme dorsal est dépendante de la rotation corticale et de la présence de VegT.
La Signalisation BMP et la Détermination du Destin Cellulaire
La mise en place des axes corporels implique également une régulation fine de la signalisation des protéines morphogénétiques osseuses (BMP). Juste avant la gastrulation, l'activité BMP établit un gradient allant d'une concentration élevée dans la région ventrale à une concentration faible dans la région dorsale. Une faible activité BMP sur la face dorsale permet aux cellules ectodermiques d'acquérir un destin neural, tandis que les autres cellules ectodermiques deviennent de l'épiderme. La culture isolée d'une calotte animale entraîne la formation d'un épiderme cilié, mais la dissociation des cellules dilue l'activité BMP et conduit à la formation de tissu neural.
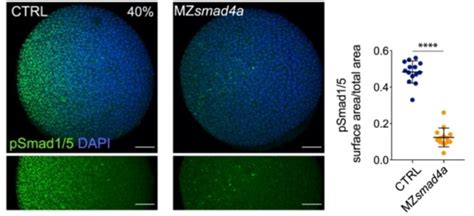
L'organisateur de Spemann joue un rôle clé dans la régulation de ce gradient BMP en sécrétant des antagonistes tels que la Chordine et la Noggin. Ces molécules se lient aux BMP et les empêchent d'interagir avec leurs récepteurs, favorisant ainsi les destins dorsaux. La Chordine, en particulier, est exprimée dans la lèvre dorsale du blastopore et dans la corde en formation. L'injection d'ARNm de Chordine peut rétablir les axes d'un embryon ventralisé par un traitement aux UV qui a perturbé la rotation corticale.
La Chordine, ainsi que d'autres inhibiteurs de morphogènes comme Dkk1, Frzb1 et Crescent, sont des exemples de molécules sécrétées par l'organisateur. Ces inhibiteurs, bien qu'ils ne soient pas des inducteurs directs, sont essentiels car ils modifient le devenir des cellules en bloquant des voies de signalisation. Ainsi, un inhibiteur de morphogène peut être considéré comme un morphogène en soi.
Chez le poisson-zèbre, la β-caténine maternelle joue également un rôle important dans la formation du bouclier embryonnaire et de l'axe DV. Des mutations affectant la β-caténine entraînent des défauts graves dans l'établissement de cet axe. La β-caténine maternelle active la transcription de gènes spécifiques dorsaux, tels que squint, goosecoid, bozozok et chordin, induisant la formation de l'organisateur de Spemann. Contrairement au xénope, c'est Wnt8a qui contribue à activer la voie Wnt/β-caténine du côté dorsal chez le poisson-zèbre.
Le nœud de Hensen chez les embryons de poulet, l'équivalent de l'organisateur de Spemann chez les amniotes, induit également la formation de tubes neuraux lorsqu'il est greffé ectopiquement. Le nœud de Hensen est une zone dynamique traversée par des cellules lors de la gastrulation et est constamment induit par un centre sécrétant cVg1 et Wnt8C. Il est même possible d'induire un "nœud de Hensen humain" à partir de cellules souches pluripotentes humaines, qui est capable d'induire du tissu neural lorsqu'il est greffé sur un embryon de poulet.
La gastrulation chez le xénope
La Polarité à l'Échelle Moléculaire et Cellulaire
La mise en place des axes corporels est un processus qui se déroule à plusieurs niveaux, de l'organisation moléculaire à la formation de structures embryonnaires complexes. Au niveau cellulaire, la division asymétrique des cellules souches, guidée par la position correcte du fuseau mitotique, est fondamentale pour assurer des destins cellulaires appropriés. Les microtubules astraux jouent un rôle dans la génération des forces nécessaires à cette organisation.
La compréhension de ces mécanismes est approfondie par l'étude de modèles animaux variés, tels que la drosophile, le ver Caenorhabditis elegans, le xénope et la souris. Bien que les détails de l'ovogenèse, de la fécondation et du développement diffèrent entre ces espèces, des thèmes communs émergent, notamment le rôle des ARNm corticaux, des protéines de polarité PAR et des réorganisations médiées par le cytosquelette.
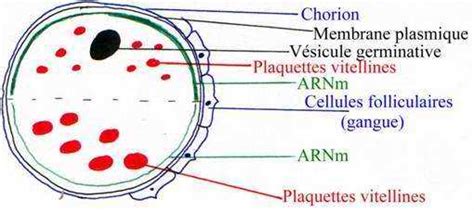
Chez le xénope, par exemple, la maturation de l'ovocyte conditionne les premières étapes de l'embryogenèse. La répartition différentielle des macromolécules dans le cytoplasme de l'ovocyte, comme les ribosomes, les protéines et les ARN, ainsi que le vitellus, établit un gradient qui sera crucial pour le développement. Des molécules importantes pour la définition des axes, souvent appelées "déterminants maternels", sont stockées dans l'ovocyte, notamment la protéine Dishevelled et les ARNm codant Vg1, VegT et Wnt11, concentrés au pôle végétatif.
La fécondation déclenche la reprise de la méiose et la rotation de symétrisation, qui déplace ces déterminants maternels vers la future zone dorsale. L'inhibition de cette rotation par des traitements aux UV conduit à des embryons sévèrement perturbés, dépourvus de structures dorsales et avec un axe antéro-postérieur raccourci, soulignant son rôle essentiel dans la mise en place des axes corporels.
La segmentation de l'œuf, qui suit la fécondation, conduit à la formation d'une masse de cellules, la morula, puis d'une structure creuse, la blastula. Les différences dans la répartition des déterminants maternels entre les cellules filles lors de ces divisions précoces sont à l'origine des premières asymétries.
L'Axe Hypothalamo-Hypophysaire : Un Autre Type d'Axe Biologique
Il est important de noter que le terme "axe" en biologie peut également faire référence à des systèmes de signalisation et de régulation hormonale. L'axe hypothalamo-hypophysaire, par exemple, est une structure neuroendocrinienne essentielle qui coordonne la communication entre le système nerveux central et le système endocrinien. Il est composé de l'hypothalamus, situé à la base du cerveau, et de l'hypophyse, une glande logée sous l'hypothalamus.
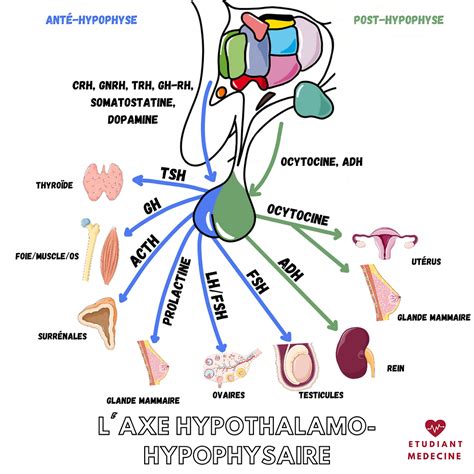
L'hypothalamus produit des hormones libératrices ou inhibitrices qui dirigent l'activité de l'hypophyse. L'hypophyse, à son tour, agit comme un relais, avec son lobe antérieur (adénohypophyse) produisant diverses hormones (comme la GH, la prolactine, l'ACTH, la TSH, la LH et la FSH) et son lobe postérieur (neurohypophyse) stockant et libérant des neurohormones hypothalamiques (ocytocine et ADH). La régulation de cet axe repose sur des mécanismes de rétrocontrôle, principalement négatif, où les hormones périphériques inhibent la production des hormones hypothalamiques et hypophysaires lorsque leurs niveaux sont suffisants.
Cet axe joue un rôle central dans la régulation de fonctions vitales telles que le stress, la croissance, le métabolisme, la reproduction et l'homéostasie. Des dérèglements de l'axe hypothalamo-hypophysaire peuvent entraîner diverses pathologies endocriniennes, nécessitant des approches thérapeutiques adaptées, allant de la substitution hormonale à la chirurgie.
Conclusion
En résumé, la notion d'axe en biologie englobe à la fois les plans fondamentaux de l'organisation corporelle lors du développement embryonnaire, tels que les axes antéro-postérieur et dorso-ventral, et les systèmes de signalisation et de régulation complexes, comme l'axe hypothalamo-hypophysaire. La mise en place des axes corporels est un processus hautement conservé et finement régulé, initié par des événements moléculaires et cellulaires précoces, tels que la rotation corticale et la signalisation Wnt, et orchestré par des centres inducteurs comme l'organisateur de Spemann. Ces mécanismes, étudiés à travers une variété de modèles animaux, révèlent les principes fondamentaux qui régissent la formation de la vie.
tags: #axe #cellulaire #court
