Les réactions acido-basiques constituent une pierre angulaire de la chimie, décrivant une classe fondamentale de transformations chimiques qui régissent de nombreux processus naturels et industriels. Au cœur de ces réactions se trouve un échange dynamique entre des entités aux propriétés opposées : les acides et les bases. Comprendre la nature de cet échange, son évolution historique et ses implications est essentiel pour appréhender le comportement de la matière à l'échelle moléculaire.
Les Fondements de la Réaction Acido-Basique : Le Transfert de Proton
Une réaction acido-basique, dans sa définition la plus couramment admise, est une réaction chimique au cours de laquelle un corps chimique ou entité dite « acide » réagit avec une entité dite « basique » et nommée base. La notion de réaction acide-base comme transfert de « proton » date de peu après 1920, date à laquelle Rutherford introduit ce nom pour décrire l’ion $\text{H}^+$ comme particule élémentaire (sans solvant).
Un acide, selon la théorie de Brønsted-Lowry, est une espèce chimique capable de céder un ou plusieurs protons ($\text{H}^+$). Par exemple, l'acide acétique ou éthanoïque de formule chimique $\text{CH}3\text{CO}2\text{H}$ est capable de céder un proton $\text{H}^+$. Les acides qui peuvent céder plusieurs protons sont appelés polyacides. L'acide citrique $\text{C}6\text{H}8\text{O}_7$, par exemple, est un triacide car il peut céder trois protons.
À l'inverse, une base, selon Brønsted-Lowry, est une espèce chimique capable de capter un ou plusieurs protons $\text{H}^+$. L'ion acétate $\text{CH}3\text{CO}2^−$, par exemple, est capable de capter un proton $\text{H}^+$ pour donner l'acide éthanoïque.
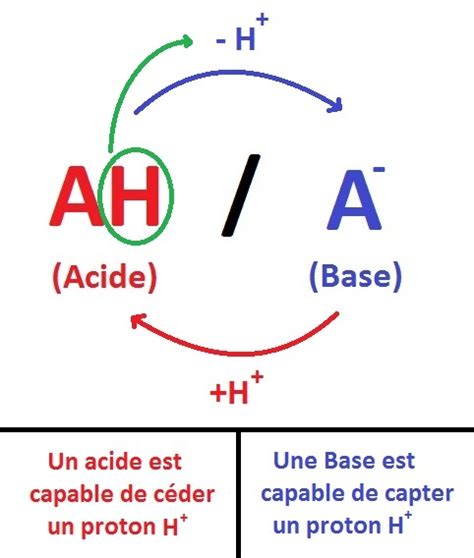
La théorie de Brønsted-Lowry, plus communément appelée théorie de Brønsted, décrit les réactions acido-basiques comme un échange de protons ($\text{H}^+$) entre deux espèces : un acide et une base. Ainsi, lorsqu’un acide $\text{AH}$ cède un proton, il produit sa base conjuguée $\text{A}^-$. Les deux espèces chimiques forment alors un couple acide/base, tel que $\text{CH}3\text{COOH/CH}3\text{COO}^-$. De même, l'acide chlorhydrique ($\text{HCl}$) et l'ion chlorure ($\text{Cl}^-$) forment le couple acide/base $\text{HCl/Cl}^-$.
L'Évolution des Concepts : De Arrhenius à Lewis
Les études sur les acides et les bases ne sont pas nouvelles. Dès le XIXe siècle, des chimistes comme Arrhenius se sont intéressés à ces espèces chimiques au comportement spécifique. La théorie d'Arrhenius, bien qu'innovante pour son époque, définissait un acide comme une substance qui se dissocie dans l'eau pour produire des ions $\text{H}^+$, et une base comme une substance qui produit des ions $\text{OH}^-$. Cependant, cette théorie présentait des limites, notamment dans son incapacité à expliquer le comportement basique de substances ne contenant pas d'ion $\text{OH}^-$, comme l'ammoniac.
Les réserves aux propositions formulées en 1921 par Joannes Brønsted et Thomas Lowry, concernant par exemple des corps chimiques singuliers comme l'ammoniac ou le trifluorure de bore, conduisent en 1923 à la théorie formulée par Gilbert Lewis. La théorie de Lewis offre une perspective plus générale et plus englobante, basée non pas sur le transfert de proton, mais sur l'échange d'un doublet électronique. Selon Lewis, un acide est une espèce qui peut accepter une paire d'électrons, tandis qu'une base est une espèce qui possède une paire d'électrons non-liante et peut l'offrir lors d'une réaction. L'interaction acide-base au sens de Brønsted peut être considérée comme un cas particulier de l'interaction électrophile-nucléophile du modèle de Lewis, où l'ion $\text{H}^+$ est l'électrophile et la base de Brønsted est le nucléophile.
Le Rôle Crucial du Solvant : Les Solvants Protiques et Aprotiques
La nature du solvant joue un rôle déterminant dans les réactions acido-basiques. Un solvant protique, comme l'eau, l'ammoniac ou le méthanol, est capable de fournir et/ou capter un ion $\text{H}^+$. Il peut ainsi agir comme acide ou comme base, ou les deux à la fois. L'eau, par exemple, est un ampholyte : elle peut agir comme base en présence d'un acide (acceptant un proton) et comme acide en présence d'une base forte (donnant un proton). La réaction d'autoprotolyse de l'eau, $\text{H}3\text{O}^+ + \text{OH}^- \rightleftharpoons 2 \text{ H}2\text{O}$, illustre parfaitement ce caractère amphotère. Les deux demi-équations associées sont $\text{H}3\text{O}^+ \rightleftharpoons \text{H}2\text{O} + \text{H}^+$ et $\text{OH}^- + \text{H}^+ \rightleftharpoons \text{H}2\text{O}$. Le produit ionique de l'eau, $[\text{H}3\text{O}^+].[\text{OH}^-] = 10^{-14}$, témoigne de cet équilibre.
D'autres solvants, comme les éther-oxydes ($\text{R-O-R}$), peuvent capter un proton mais ne peuvent pas en donner ; ils sont dits solvants aprotiques polaires. Des solvants comme le benzène ou le pentane ne peuvent ni donner ni accepter de proton et sont qualifiés de solvants aprotiques apolaires.
L'Amphotérisme : La Dualité des Espèces Chimiques
Certaines espèces chimiques possèdent la capacité de se comporter à la fois comme un acide ou comme une base, selon le milieu réactionnel. Ces substances sont qualifiées d'ampholytes, ou dites amphotères. L'eau en est l'exemple le plus emblématique. Les zwitterions, qui possèdent deux charges électriques opposées sur des groupes distincts ou des atomes non adjacents, sont également des exemples d'espèces amphotères en raison de leur structure moléculaire particulière.
L'Échelle de pH : Quantifier l'Acidité et la Basicité
En solution aqueuse, l'acidité ou la basicité d'une solution est quantifiée par le pH. Le pH est défini comme la valeur négative du logarithme décimal de l'activité des ions hydronium ($\text{H}3\text{O}^+$). Dans des solutions suffisamment diluées, où les interactions entre ions sont négligeables, l'activité peut être approximée par la concentration molaire. Le pH est ainsi plus simplement exprimé comme étant la valeur négative du logarithme décimal de la concentration molaire (C, mol/L) en ions hydronium notée $[\text{H}3\text{O}^+]$. Le pH n'a pas d'unité.
L'usage du logarithme pour définir le pH n'est pas arbitraire. Les concentrations en ions $\text{H}_3\text{O}^+$ peuvent varier sur plusieurs ordres de grandeur, rendant leur visualisation directe sur un graphique difficile. Une échelle logarithmique s'impose alors pour toute représentation lisible. De plus, les calculs d'équilibres chimiques en solution aqueuse font largement appel aux logarithmes, renforçant la pertinence de cette définition.
Dans le cadre de la théorie de Brønsted-Lowry, les acides sont reconnaissables en solution aqueuse par un pH inférieur à 7, tandis que les bases présentent un pH supérieur à 7. Un pH égal à 7 indique une solution neutre.
Définition et mesure du pH
Les Couples Acide-Base et les Constantes d'Acidité
Les acides et les bases peuvent être regroupés en couples acide/base. Un acide, en perdant un proton, produit sa base conjuguée, qui est capable de capter un proton. La réaction $\text{Acide} \rightleftharpoons \text{Base} + \text{H}^+$ est une réaction équilibrée. La constante d'équilibre de cette réaction, notée $\text{Ka}$, est souvent exprimée sous sa forme logarithmique négative : $\text{pKa} = -\log_{10}(\text{Ka})$. Plus le $\text{pKa}$ est élevé, plus l'acide est faible. Un acide fort est un acide dont le $\text{pKa}$ est négatif ; sa dissolution dans l'eau est considérée comme totale.
La position de l'équilibre dans une réaction acido-basique est dépendante des valeurs de $\text{pKa}$ des couples concernés. La règle du gamma permet de visualiser la réaction prépondérante : acide fort + base forte $\rightarrow$ base conjuguée faible + acide conjuguée faible. Lorsque le pH d'une solution est égal au $\text{pKa}$ d'un couple acide/base, cela signifie que l'on a un mélange égal entre l'acide et sa base conjuguée.
Exemples Concrets de Réactions Acido-Basiques
De nombreuses molécules illustrent les principes des réactions acido-basiques. L'ion oxalate $\text{C}2\text{O}4^{2-}$ est une dibase susceptible de réagir avec deux ions $\text{H}^+$. L'acide oxalique $\text{H}2\text{C}2\text{O}4$ (HOOC-COOH, acide éthanedioïque) est un diacide qui peut se dissocier en libérant deux ions $\text{H}^+$. L'acide phosphorique $\text{H}3\text{PO}_4$ est un triacide capable de libérer trois ions $\text{H}^+$.
Les acides carboxyliques de formule générale $\text{R-COOH}$ sont des acides de Brønsted cédant un proton pour former l'ion carboxylate $\text{R-COO}^-$. Les amines, dont la formule générale est $\text{R}3\text{N}$, $\text{R}2\text{NH}$ ou $\text{RNH}2$, sont des bases de Brønsted capables de capter un proton pour former l'ion ammonium correspondant ($\text{R}3\text{NH}^+$, $\text{R}2\text{NH}2^+$ ou $\text{RNH}_3^+$).
Un exemple concret de réaction acido-basique est la mise en présence d'une solution acide de chlorure d'ammonium ($\text{NH}4^+(\text{aq}), \text{Cl}^-(\text{aq})$) et d'une solution basique de soude ($\text{Na}^+(\text{aq}), \text{HO}^-(\text{aq})$). On observe un dégagement gazeux d'ammoniac ($\text{NH}3$). Les ions $\text{Na}^+$ et $\text{Cl}^-$ sont des ions spectateurs ne participant pas à la réaction. L'équation-bilan est : $\text{NH}4^+(\text{aq}) + \text{HO}^-(\text{aq}) \rightleftharpoons \text{NH}3(\text{g}) + \text{H}_2\text{O}(\text{l})$.
La Théorie de Lewis : Une Vision Plus Large
Bien que la théorie de Brønsted-Lowry soit largement utilisée, la théorie de Lewis offre une définition plus générale des acides et des bases. Un acide de Lewis est une espèce qui peut accepter une paire d'électrons, tandis qu'une base de Lewis est une espèce qui peut fournir une paire d'électrons. Cette approche permet de décrire des réactions qui ne font pas intervenir de transfert de proton, comme la réaction entre l'ion cuivreux ($\text{Cu}^{2+}$), un acide de Lewis, et l'ammoniac ($\text{NH}_3$), une base de Lewis, pour former un complexe. Cette interaction électrophile-nucléophile est fondamentale pour comprendre une vaste gamme de réactions chimiques.
Les réactions acido-basiques, qu'elles soient décrites par le modèle de Brønsted-Lowry ou par celui de Lewis, sont essentielles pour comprendre la chimie des solutions, la catalyse, et de nombreux processus biologiques et environnementaux. Leur étude révèle une danse moléculaire complexe mais fascinante d'échanges et d'interactions qui façonnent le monde qui nous entoure.
tags: #chap #reaction #acido #basique #term
