L'adénosine monophosphate cyclique, plus communément appelé AMPc, est une molécule biologique d'une importance capitale, agissant comme un second messager intracellulaire. Son rôle est central dans la transmission de signaux initiés par des hormones ou des neurotransmetteurs, orchestrant ainsi une myriade de processus physiologiques au sein des organismes vivants. La découverte et la compréhension approfondie de ses mécanismes d'action ont valu à Earl W. Sutherland, Jr. le prix Nobel de physiologie et de médecine en 1971, pour ses travaux pionniers sur la manière dont les hormones exercent leurs effets, démontrant clairement l'existence et le rôle de l'AMPc, notamment dans la libération de glucose en réponse au stress.
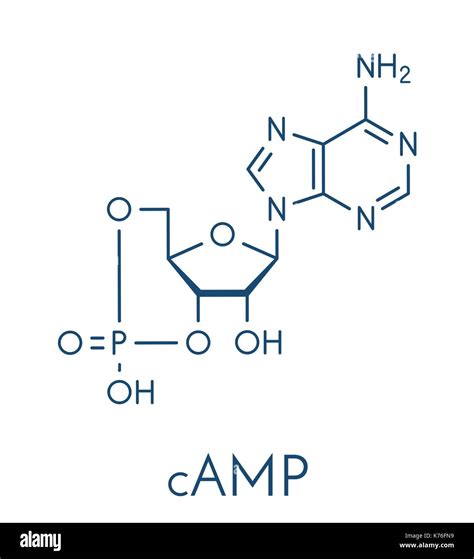
Synthèse et Dégradation de l'AMPc : Un Équilibre Dynamique
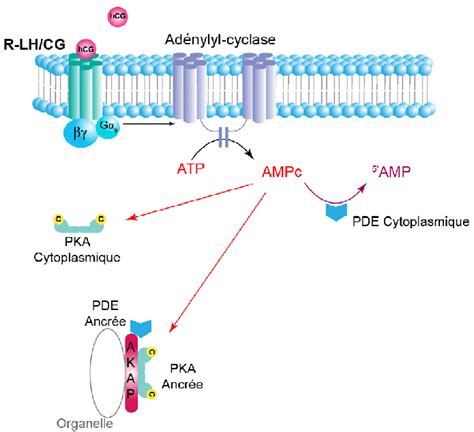
Au sein des êtres vivants, la synthèse de l'AMPc s'effectue à partir de l'ATP, sous l'action de l'enzyme adénylate cyclase (également appelée adényl cyclase). Cette enzyme est typiquement activée ou réprimée en réponse à la liaison d'un ligand - qu'il s'agisse d'une hormone ou d'un neurotransmetteur - à un récepteur spécifique, souvent caractérisé par ses sept domaines transmembranaires et couplé à une protéine G hétéro-trimérique. En parallèle, l'AMPc peut être dégradé par une autre enzyme, la phosphodiestérase, assurant ainsi un contrôle précis de sa concentration intracellulaire et, par conséquent, de l'intensité du signal.
Mécanismes d'Action de l'AMPc : Activation et Modulation
L'AMPc exerce ses fonctions principalement en activant des enzymes clés, la plus notable étant la Protéine Kinase A (PKA). La PKA, une fois activée par l'AMPc, phosphoryle diverses protéines cibles, modifiant ainsi leur activité ou leur localisation. Ce processus de phosphorylation est un mécanisme fondamental de régulation cellulaire. L'AMPc peut également moduler directement les propriétés de certaines protéines par interaction physique. C'est le cas, par exemple, des canaux ioniques HCN (Hyperpolarization-activated Cyclic Nucleotide-gated channels). En présence d'AMPc, la courbe d'activation du courant Ih, médié par ces canaux, est décalée, ce qui signifie qu'une moindre hyperpolarisation suffit à activer plus rapidement les canaux HCN. D'autres canaux ioniques, tels que les canaux CNG (Cyclic Nucleotide-gated channels), peuvent également être activés par l'AMPc.
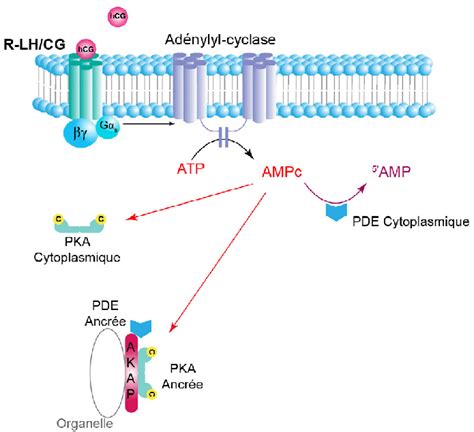
L'AMPc dans la Signalisation Cellulaire : Diversité des Rôles
La portée de l'AMPc s'étend bien au-delà de la simple activation de la PKA. Il est impliqué dans une multitude de voies de signalisation, influençant des processus aussi variés que le métabolisme, la contraction musculaire, la neurotransmission, et même le comportement cellulaire.
Signalisation Cardiaque : Modulation de la Contraction
Au niveau des cellules myocardiques, la liaison d'un agoniste β-adrénergique à son récepteur spécifique (un récepteur à sept domaines transmembranaires) entraîne une stimulation de l'adénylate cyclase via une protéine G hétéro-trimérique (Gαβγ). L'augmentation subséquente de l'AMPc conduit à une activation de la Protéine Kinase A (PKA). La PKA, à son tour, module l'activité du canal calcique voltage-dépendant (VOC), influençant ainsi l'entrée de calcium dans la cellule et, par conséquent, la force et la fréquence des contractions cardiaques.
Signalisation Musculaire Lisse : Relaxation
À l'inverse, dans les cellules musculaires lisses, un agoniste β-adrénergique (ou toute autre substance capable d'augmenter l'AMPc) entraîne une phosphorylation de la "myosin light chain kinase" (MLCK). Cette phosphorylation a pour conséquence l'inactivation de la MLCK, ce qui réduit la phosphorylation de la myosine et conduit à la relaxation du muscle lisse. Ce mécanisme est crucial pour la régulation du tonus vasculaire, par exemple.
Signalisation via les Récepteurs Couplés aux Protéines G et les Récepteurs à Tyrosine Kinase
La liaison d'agonistes comme l'angiotensine II ou la thrombine à leurs récepteurs à sept domaines transmembranaires active une phospholipase C (PLCβ) par l'intermédiaire des protéines Gαβγ. Cette activation conduit à la production de deux seconds messagers : le diacylglycérol (DAG), qui reste dans la membrane et active une protéine kinase C dépendante du Ca2+, et l'inositol triphosphate (IP3), qui diffuse dans le cytosol et se fixe sur des récepteurs IP3-dépendants situés sur le réticulum endo/sarcoplasmique, provoquant la libération de calcium.
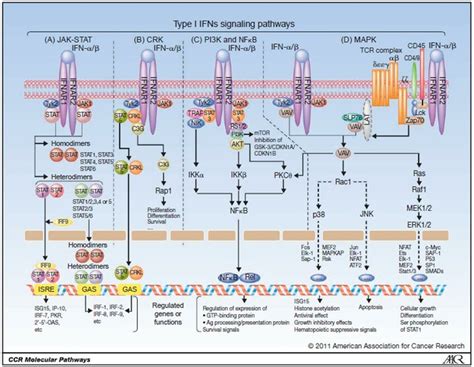
Par ailleurs, la liaison de facteurs de croissance tels que l'EGF (Epidermal Growth Factor) ou le PDGF (Platelet-Derived Growth Factor) à des récepteurs à activité tyrosine kinase déclenche une cascade de signalisation différente. L'auto-phosphorylation des sites intracellulaires du récepteur, souvent accompagnée d'une dimérisation, entraîne une modification de sa structure. Cette modification permet une interaction directe avec la PLCγ, sans impliquer de protéines G. L'activation de la PLCγ conduit alors à l'hydrolyse du PIP2, générant également du DAG, de l'IP3 et du Ca2+.
L'AMPc comme Chimioattracteur
Il est également intéressant de noter que l'AMPc peut jouer un rôle de chimioattracteur. Dans le cas d'organismes sociaux comme les amibes Dictyostelium discoideum, l'AMPc est libéré dans l'environnement et guide les autres amibes vers la source, facilitant ainsi la formation d'agrégats cellulaires.
L'AMPc dans la Régulation de la Reproduction : Le Cas des Ovocytes
Des recherches récentes ont mis en lumière le rôle fascinant de l'AMPc dans la régulation de processus aussi fondamentaux que la division cellulaire, en particulier lors de l'ovogenèse. Les cellules se multiplient par divisions répétées, un processus essentiel à la croissance et à la reproduction de tous les êtres vivants. Chez les ovocytes, ces divisions, appelées divisions méiotiques, sont finement régulées par des hormones.
Les blocages de la méiose lors de l'ovogenèse
Dans le cadre du projet OOCAMP, l'étude des ovocytes du xénope (un amphibien) et de la méduse Clytia a révélé un paradoxe surprenant concernant le rôle de l'AMPc. Chez le xénope, la division méiotique est déclenchée par une chute de la concentration d'AMPc dans l'ovocyte. À l'inverse, chez la méduse Clytia, c'est une hausse de l'AMPc qui est nécessaire pour permettre la reprise de la division. Cette divergence d'action souligne la complexité et l'adaptabilité des voies de signalisation.
Les chercheurs ont abordé ce paradoxe en comparant les molécules régulatrices en amont et en aval de l'AMPc chez ces deux espèces. Chez le xénope, il a été découvert que la protéine ARPP19 est une cible clé de la PKA. Cette protéine, une fois phosphorylée par la PKA, est responsable du maintien de l'état de dormance des ovocytes. Cependant, sous l'influence d'une autre enzyme, la kinase Greatwall (Gwl), une phosphorylation distincte de l'ARPP19 la transforme en un activateur du MPF (M-phase Promoting Factor), un complexe protéique essentiel à l'entrée en division. L'homologue d'ARPP19 a été identifié chez Clytia, et ses sites de phosphorylation par PKA et Gwl ont été étudiés pour comprendre les différences fonctionnelles.
En amont de l'AMPc, le projet OOCAMP a permis d'identifier chez Clytia l'hormone responsable de la reprise de la méiose et son récepteur ovocytaire, ainsi qu'une protéine photoréceptrice qui régule la production de cette hormone. Ces découvertes, basées sur des approches de transcriptomique, de tests fonctionnels in vitro et de mutation dirigée par CRISPR-Cas9, ont considérablement enrichi notre compréhension des systèmes biochimiques qui relient les signaux extracellulaires de maturation méiotique à l'activation du MPF. Ces recherches ont fait évoluer les concepts de la méiose, introduisant de nouveaux paradigmes tels que le passage de la notion de bascule à celle de rhéostat, et l'utilisation divergente de l'AMPc entre invertébrés et vertébrés.
L'AMPc dans le Métabolisme : Régulation Énergétique
L'AMPc joue un rôle prépondérant dans la régulation du métabolisme énergétique, notamment celui des glucides et des lipides.
Métabolisme des Glucides
Dans le métabolisme des glucides, l'AMPc facilite la mobilisation du glucose. Il stimule la dégradation du glycogène hépatique en glucose, ainsi que la gluconéogenèse (la synthèse de glucose à partir de précurseurs non glucidiques) dans le foie. Ces processus sont principalement induits par des hormones comme le glucagon et les catécholamines (adrénaline, noradrénaline) en situation de besoin énergétique accru. Chez les mammifères, le signal AMPc déclenche des programmes métaboliques dans les tissus sensibles à l'insuline, tels que le foie, le muscle squelettique et le tissu adipeux. Cette régulation implique des facteurs de transcription comme CREB (cAMP Response Element-Binding protein) et des coactivateurs qui modulent l'expression des gènes impliqués dans le métabolisme du glucose.
Métabolisme des Lipides
Dans le tissu adipeux, l'AMPc favorise la lipolyse, c'est-à-dire la dégradation des triglycérides stockés en acides gras libres et glycérol. Ces acides gras sont ensuite libérés dans la circulation sanguine pour être utilisés comme source d'énergie par d'autres tissus.
Outils de Recherche : Dosage de l'AMPc
Pour étudier le rôle de l'AMPc dans ces divers processus, les chercheurs disposent de kits de dosage modernes. Ces kits permettent de quantifier avec précision les concentrations d'AMPc dans une large gamme d'échantillons biologiques, incluant le sérum, le plasma, l'urine, les lysats tissulaires et les milieux de culture cellulaire. Ces outils sont indispensables en recherche métabolique, car ils permettent une quantification sensible et spécifique de l'AMPc, facilitant ainsi la compréhension de ses rôles multiples et de la régulation des métabolismes des glucides et des lipides, de l'action hormonale et de l'équilibre énergétique cellulaire. Les études récentes en protéomique et métabolomique continuent d'élargir la compréhension de l'influence de l'AMPc sur des réseaux métaboliques encore plus vastes.
Conclusion
En somme, l'adénosine monophosphate cyclique est une molécule centrale dans la signalisation cellulaire, agissant comme un intermédiaire crucial entre les stimuli externes et les réponses internes. Ses rôles variés, de la modulation de la contraction cardiaque à la régulation de la reproduction et du métabolisme, témoignent de son importance fondamentale pour la vie. La recherche continue d'explorer les subtilités de ses voies de signalisation, promettant de nouvelles découvertes et une meilleure compréhension des processus physiologiques et pathologiques.
tags: #ampc #marqueur #cellulaire
