La prolifération cellulaire, processus fondamental de la vie, désigne l'augmentation du nombre de cellules résultant de la division cellulaire. Ce mécanisme, loin d'être aléatoire, est finement contrôlé et joue un rôle crucial dans le développement, la réparation des tissus et le maintien de l'homéostasie des organismes vivants. Comprendre la prolifération cellulaire est donc essentiel pour appréhender des domaines aussi variés que l'embryogenèse, la cicatrisation des plaies, et des pathologies complexes telles que le cancer.
Définition et Concepts Clés de la Prolifération Cellulaire
Au sens le plus simple, la prolifération cellulaire est le processus par lequel une cellule se divise et se multiplie, augmentant ainsi le nombre total de cellules au sein d'un organisme. Ce n'est pas simplement une question de multiplication, mais d'un équilibre subtil entre les divisions cellulaires et la perte cellulaire par mort ou différenciation. La prolifération cellulaire est intrinsèquement liée à la croissance cellulaire et à la division cellulaire, bien que ces termes ne soient pas interchangeables. La croissance cellulaire se réfère à l'augmentation de la taille d'une cellule, tandis que la division cellulaire est le processus par lequel une cellule mère se sépare en deux cellules filles. La prolifération cellulaire implique généralement une coordination de ces deux processus pour maintenir une taille de cellule relativement constante au sein d'une population en croissance exponentielle.
Les concepts clés à retenir incluent :
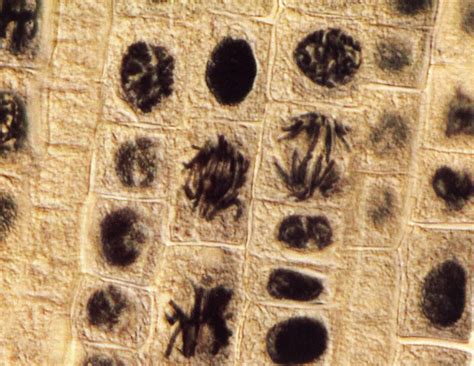
- Cycle cellulaire : Une séquence ordonnée d'événements qui mènent à la duplication de la cellule et à sa division. Il comprend généralement quatre phases : G1 (croissance initiale), S (réplication de l'ADN), G2 (préparation à la mitose) et M (mitose et division cellulaire).
- Facteurs de croissance : Des protéines signalétiques qui se lient aux récepteurs de surface cellulaire, déclenchant des cascades de signalisation internes qui encouragent la croissance et la division cellulaire. Des exemples incluent les facteurs de croissance des fibroblastes (FGF) et le facteur de croissance épidermique (EGF).
- Indice de prolifération : Une mesure quantitative de l'activité mitotique dans une population cellulaire, souvent exprimée en pourcentage de cellules en division active.
La prolifération cellulaire est un processus complexe, étroitement contrôlé et bien défini dans l'organisme. Son rôle est crucial, par exemple, dans la réparation des tissus suite à une lésion toxique. Dans une population de cellules, l'activité de prolifération peut être décrite au moyen de la densité de probabilité pour une protéine de prolifération, comme la forme phosphorylée de la kinase régulée par le signal extracellulaire (ERK).
Mécanismes Régissant la Prolifération Cellulaire
La régulation de la prolifération cellulaire est orchestrée par des mécanismes sophistiqués qui assurent la fidélité de la division cellulaire et répondent aux besoins de l'organisme. Ces mécanismes impliquent une interaction complexe entre des voies de signalisation multiples et des systèmes de surveillance du stress.
Le Cycle Cellulaire : Une Danse Moléculaire Précise
Le cycle cellulaire est le pilier de la prolifération. Sa progression est assurée par l'activation et l'inhibition cycliques de complexes protéiques appelés cyclines et kinases dépendantes des cyclines (CDK). Ces complexes agissent comme des gardiens, s'assurant que chaque étape est complétée avant de passer à la suivante.
- Phase G1 : La cellule croît et se prépare à la réplication de l'ADN. La durée de cette phase est particulièrement modulable et peut être influencée par la taille de la cellule (modèle "sizer") ou par un incrément de taille constant (modèle "adder").
- Phase S : La réplication de l'ADN a lieu, produisant deux copies identiques du génome.
- Phase G2 : La cellule continue de croître et se prépare à la mitose.
- Phase M : La mitose (division du noyau) et la cytokinèse (division du cytoplasme) aboutissent à la formation de deux cellules filles.
Contrôle de la Taille Cellulaire : Une Nécessité pour la Division
La taille d'une cellule est un paramètre finement régulé. Les cellules doivent croître pour doubler leur volume avant de se diviser. Cette croissance est coûteuse en énergie et dépend du métabolisme de base de la cellule. Des contraintes physiques, comme la capacité d'échange avec le milieu extérieur et la diffusion moléculaire, influencent également la taille cellulaire.
Pour maintenir une taille constante au cours des générations, les cellules utilisent différents mécanismes :
- Modèle "Sizer" : La cellule se divise une fois qu'elle atteint une taille critique. La durée du cycle est ajustée pour que les cellules plus petites aient une phase G1 plus longue.
- Modèle "Adder" : La cellule se divise après avoir augmenté sa taille d'un volume fixe, indépendamment de sa taille initiale.
La mesure de la taille cellulaire est souvent réalisée par la titration de la concentration d'une protéine inhibitrice du cycle cellulaire. Sa concentration diminue au fur et à mesure que la cellule grandit, et lorsqu'elle atteint un seuil critique, le cycle peut progresser.
Rôle des Complexes Protéiques dans la Régulation
Des découvertes récentes ont mis en lumière le rôle de complexes protéiques dans la régulation de la prolifération. Les équipes scientifiques de l'INRA, de l'École Normale Supérieure de Lyon et du CNRS ont utilisé Arabidopsis thaliana (une plante) et Drosophila melanogaster (la mouche du vinaigre) pour étudier la protéine TCTP. Ils ont découvert que TCTP interagit avec CSN4, un membre du complexe COP9. Ce complexe est connu pour réguler de nombreux processus cellulaires, y compris le cycle cellulaire, via la régulation d'un autre complexe, les CULLIN-RING E3 ubiquitin ligases (CRLs). Chez Arabidopsis, TCTP détourne la fonction de COP9, séquestrant CSN4 et rendant ainsi le complexe COP9 inactif lors de l'entrée des cellules en division. Ce mécanisme affecte spécifiquement la régulation du cycle cellulaire, la division cellulaire et la formation des organes.
La Prolifération Cellulaire dans des Contextes Physiologiques et Pathologiques
La prolifération cellulaire est à la fois un moteur de la vie et une cible potentielle de maladies.
Développement et Réparation Tissulaire
Dès l'embryogenèse, la prolifération cellulaire est essentielle à la formation des organes et des structures. Par la suite, elle joue un rôle clé dans la réparation des tissus suite à des blessures ou des agressions. La cicatrisation des plaies, par exemple, dépend d'une prolifération coordonnée des cellules environnantes pour remplacer les tissus endommagés.
Cancer : La Prolifération Incontrôlée
À l'inverse, une prolifération cellulaire anormale et incontrôlée est la signature du cancer. Les cellules cancéreuses échappent aux mécanismes de régulation normaux, se divisant de manière exponentielle et formant des tumeurs. Le gène TCTP, identifié dans les recherches sur le cancer, est fortement surexprimé dans de nombreuses cellules cancéreuses et serait impliqué dans les mécanismes de développement et de prolifération tumorale.
Hématopoïèse Clonale et Maladies Cardiovasculaires
L'hématopoïèse clonale, une condition où des clones individuels de cellules souches hématopoïétiques génèrent une fraction disproportionnée de leucocytes sanguins, est corrélée à un risque accru de maladie cardiovasculaire. Les taux de division des cellules souches hématopoïétiques sont augmentés chez les souris et les humains atteints d'athérosclérose. L'augmentation de la prolifération des cellules souches accélère l'évolution somatique et l'expansion des clones avec des mutations conductrices.
Stress Oxydatif et Régulation du Cycle Cellulaire
En réponse au stress oxydatif, les cellules s'arrêtent dans le cycle cellulaire. Un contrôle redox aberrant de la prolifération sous-tend la pathogenèse de nombreuses maladies, y compris le cancer et les troubles neurodégénératifs. La détection redox de la régulation du cycle cellulaire implique des thiols de cystéine réactifs qui fonctionnent comme des capteurs redox dans les régulateurs du cycle cellulaire.
Techniques d'Analyse et d'Ingénierie de la Prolifération Cellulaire
L'étude et la manipulation de la prolifération cellulaire reposent sur un éventail de techniques sophistiquées.
Culture Cellulaire : Un Laboratoire In Vitro
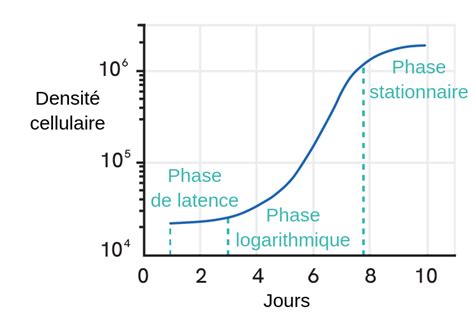
La culture cellulaire permet d'étudier la prolifération dans un environnement contrôlé. Les cellules sont maintenues dans des milieux nutritifs, souvent enrichis en facteurs de croissance pour stimuler leur croissance. Des systèmes automatisés comme le système de surveillance de l'incubation CM20 permettent un suivi en temps réel de la prolifération et de la confluence des cellules, offrant des données quantitatives fiables. Ces systèmes permettent d'observer des courbes de croissance, souvent sigmoïdes, qui révèlent les phases de latence, de croissance exponentielle et de plateau.
Analyse de la Prolifération : Mesurer l'Activité
Plusieurs méthodes sont utilisées pour évaluer la prolifération :
- Tests basés sur l'activité métabolique : Des kits comme le WST-8 ou la mesure de l'ATP quantifient la prolifération en se basant sur le métabolisme cellulaire.
- Tests basés sur la synthèse d'ADN : Les tests au BrdU ou à la thymidine mesurent le taux de synthèse d'ADN, un indicateur de la division cellulaire.
- Comptage cellulaire direct : Des systèmes automatisés ou des méthodes manuelles permettent de compter le nombre de cellules.
- Marqueurs de prolifération : L'utilisation de marqueurs comme Ki-67, une protéine exprimée dans les phases actives du cycle cellulaire (G1, S, G2, M), permet d'identifier les cellules en division. La cytométrie en flux est une technique couramment utilisée pour analyser la prolifération cellulaire à l'aide de marqueurs comme CFSE ou Ki-67.
Manipulation Génétique et Ingénierie Tissulaire
Les outils de manipulation génétique, tels que CRISPR-Cas9, permettent de modifier spécifiquement les gènes régulant la prolifération cellulaire. L'ingénierie tissulaire combine ces approches pour créer des tissus fonctionnels, en optimisant les matrices et en utilisant des facteurs biochimiques et physiques pour contrôler la croissance cellulaire. L'application de modèles mathématiques est essentielle pour comprendre et prédire le comportement cellulaire sous diverses influences, y compris les mutations génétiques.
Un exemple concret de suivi de la prolifération est l'utilisation du système CM20 pour observer le comportement de cellules A549 traitées au 5-FU. Dans le groupe non traité, les cellules deviennent confluentes après environ 72 heures, tandis que dans le groupe traité, la prolifération et la mort cellulaire sont en équilibre. De même, pour les cellules SH-SY5Y traitées au 6-OHDA, le système CM20 a montré une diminution rapide du nombre de cellules, indiquant une mort cellulaire significative.
Cycle cellulaire
Défis et Implications Futures
La compréhension et le contrôle de la prolifération cellulaire présentent des défis et ouvrent des perspectives prometteuses.
Défis Éthiques et Techniques
L'utilisation de lignées cellulaires, comme les cellules HeLa issues d'Henrietta Lacks, soulève des questions éthiques importantes. De plus, les conditions de culture cellulaire, bien que contrôlées, peuvent différer des environnements physiologiques, et les propriétés des organisations 3D peuvent être perdues dans les cultures 2D classiques. Les chercheurs doivent également veiller à la pureté des cultures et éviter la contamination, par exemple par le mycoplasme, qui peut fausser les résultats.
Applications Thérapeutiques et de Recherche
La maîtrise de la prolifération cellulaire est au cœur du développement de traitements contre le cancer, visant à inhiber la division des cellules tumorales. En médecine régénérative, elle permet de développer des thérapies pour réparer ou remplacer des tissus endommagés et améliorer la cicatrisation. Les études sur la prolifération cellulaire contribuent à une meilleure compréhension des maladies dégénératives et ouvrent la voie à de nouvelles stratégies thérapeutiques.
L'utilisation de technologies comme le système CM30 permet de recueillir à distance des données quantitatives fiables sur la viabilité, la numération et la confluence des cellules en culture, facilitant ainsi la recherche et le développement. La normalisation des données, essentielle pour comparer les expériences, implique souvent de référer les résultats à un point de référence temporel (T0) ou à un contrôle du véhicule, tout en tenant compte des variations potentielles dues à la saturation de l'essai, à des effets métaboliques ou à des contaminations.
En définitive, la prolifération cellulaire demeure un domaine de recherche dynamique, dont les avancées continuent de remodeler notre compréhension de la biologie et d'ouvrir de nouvelles avenues pour la santé humaine.
tags: #courbe #de #proliferation #cellulaire
